- Otro punto a realizar en nuestra reanimación en paciente en shock con «apellido» o indiferenciado. Tocaremos los puntos más importantes al respecto además de la evidencia que hay al respecto.
Generalidades.
- Aparecen los primeros vasopresores en los 40’s.
- Recordar –> 1 episodio de hipotensión (PAM < 60) en las primeras 24 horas del Shock se asocia a un riesgo de muerte 3 veces mayor, ** la hipotensión casi siempre es mala, en shock, en ACV, en pacientes en Hemodialisis y en trauma: la hipotensión permisiva está descrita en 1 hora solamente.**
- En Sepsis: Se deben iniciar vasopresores si, después de la reanimación con fluidos, persiste la PAM < 60 mmHg o disminución de 30 mmHg del basal (Intensive Care Med DOI 10.1007/s00134-017-4683-6).
- Uso racional: TODOS tienen otros efectos que pueden ser deletereos, evaluar efectos en el consumo de O2, vasodilatación refleja, etc. Además debemos tener en cuenta la curva dosis-respuesta y las acciones directas y reflejas.
Mecanismos Fisiológicos.
- Actividad α-1: Localizados en la pared vascular –> Vasoconstricción, además localizados en el corazón –> Aumentan duración de contracción sin aumentar el cronotropismo con mecanismo no claro.
- Actividad β-1: Localizados en el corazón –> incrementan inotropismo y cronotropismo con vasoconstricción mínima. β-2 –> Vasodilatación.
- Dopamina: Receptores localizados a nivel renal, circulación esplácnica, coronaria, circulación cerebral –> Vasodilatación. Otros subtipos de receptores de Dopamina a la estimulación –> Liberación de Norepinefrina.
- Sensibiladores del Calcio: Incrementan la sensibilidad de la contracción miocárdica a través del calcio, incrementando la tensión de los miofilamentos y mejorando contractilidad. Otra propiedad farmacológica –> Inhibidores de la Fosfodiesterasa, que puede incrementar inotropismo y generar vasodilatación que ayuda al perfil clínico.
- Angiotensina: Receptores AT1 y AT2 se unen con proteinas más Angiotensina II –> Vasoconstrictor como parte del sistema RAA –> Estímulo –> Aumento de concentraciones de Calcio a nivel intracelular –> Efectos de Vasoconstricción mediado por secreción de Vasopresina y Aldosterona (Am J Physiol 1994; 266:H2462).
Ahora bien…pero, ¿cómo actúan estos fármacos? Lo mínimo que debemos conocer son los mecanismos a nivel arterial, venoso, corazón y algunos otros efectos.
Sistema Arterial:
- A modo general: Vasopresores = Vasoconstricción//Inótropos = Contractilidad, la mayoría genera ambos efectos. Efectos alfa predominan en la musculatura lisa vascular provocando incremento de calcio intracelular y por consecuencia, vasoconstricción intensa e incremento de presión sanguínea sistémica. Las arteriolas pequeñas suplen la resistencia de la alta presión sistémia y esto lleva a una adecuada autoregulación. Si la presión sistémica arterial cae al mínimo permitido, sabemos que cae la perfusión. Los vasoconstrictores ayudan al incremento de la resistencia y presión a nivel de arterial y arteriolar, con esto mejora la autoregulación, restaurando la perfusión crítica.
Sistema Venoso:
- Normal: 2/3 del volumen sanguíneo total se encuentra a nivel venoso. Venoconstricción con el uso de vasopresores con actividad alfa y vasopresina. Hay una reserva venosa que tiene control autonómico, que es independiente de la presión generada por la contracción cardiaca y está determinado por todo el volumen de sangre circulante. Esto es llamado la Presión media de llenado sistémico (PMLS) que refleja el volumen efectivo circulante, independiente de la función cardiaca, valor normal aproximado de 7 mmHg. Esta presión debe ser mayor que la Presión de Auricula Derecha (presión 0 mmHg en diastole inicial) para que pueda retornar al corazón. Así, el Retorno Venoso (RV) depende del gradiente de presión entre la Presión media de llenado sistémico y la Aurícula Derecha. La respuesta normal al aumento del RV es el incremento del Gasto Cardiaco (Ley Frank-Starling y mecanismos reflejos autonómicos) que es independiente de la estimulación cardiaca (mecanismo similar al de desafios de volumen).
-
**Los vasopresores juegan un rol esencial en la regulación del Retorno Venoso e incremento de la PMLS, incrementando el gradiente de presión y llevando el flujo hacia el corazón**.
A nivel Cardiaco:
- Al estimular receptores β-1 –> Incremento de contractilidad de miocitos cardiacos, esto ocurre por aumento de AMPc y de Calcio intracelular. Mejoría de contractilidad –> mejora «stroke volume» y reduce volumenes y presiones de llenado de fin de diastole. Ahora bien, los beta agonistas sólo generan un leve incremento en el Gasto Cardiaco en condiciones normales. El incremento mayor se ve cuando hay un volumen de fin de diastole anormal, por ejemplo en disfunción miocárdica. Además β-1 aumenta el cronotropismo y β-2 el inotropismo. La activación de β-2 –> relaja musculatura lisa –> vasodilatación arterial periférica.
- Los vasopresores además aumentan la perfusión coronaria. Sístole –> altas presiones generadas por la contracción ventricular compromen las arterias coronarias a través de las paredes del miocardio creando flujo retrogrado y anterógrado que depende del gradiente de presión entre la aorta y los ventrículos. Un GC bajo, baja la perfusión coronaria, baja el índice cardiaco que puede ocurrir en Shock Cardiogénico y también en Shock Obstructivo. En este escenario los vasopresores puede incrementar el tono vascular, restaura la presión arterial sistémica, preservan el gradiente de perfusión coronaria y finalmente, minimiza la isquemia miocárdica (modelos experimentales en TEP, Taponamiento, Shock Cardiogénico con isquemia ventricular izquierda).
-
Beneficios a este nivel: 1.- Incremento de Presión Arterial Sistémica que ayuda en la autoregulación. 2.- Aumenta RV. 3.- Aumenta contractilidad cardiaca anormal. 4.- Aumenta el gradiente de perfusión coronaria.
Otros Efectos:
- Algunos agentes –> Constricción de Arteria Pulmonar e incremento de Resistencia Vascular Pulmonar, ojo con el VD.
- Epinefrina –> Hiperglicemia e hiperlactatemia, eliminación de Potasio por la orina mayor e incremento del débito urinario independiente del efecto sobre el GC y PA.
Ahora bien, ¿cúal inicio, en quien, cómo, en qué dosis? lo veremos en base a la evidencia disponible y el perfil de cada uno.
- ¿Cuando iniciar? Se describe habitualmente si, a pesar de la volemización previa con Cristaloides persiste PAM < 60 mmHg y además el enfermo tiene un intravascular apropiado post reanimación con fluidos (esto se puede medir con ECO, PVC, PLR, Delta PP, Fluid Challenge, etc) clásicamente llamado «no respondedor».
- ¿En qué momento? Se describe que los pacientes que iniciar antes (2 horas de Shock como corte) la reanimación con DVA tienen menor mortalidad (30% vs 43%), además se constata que también por cada hora de retraso de inicio, aumenta un 5,3% la mortalidad (Crit Care 2014; 18:532).
- ¿Cuál iniciar? En base a la evidencia y guías en cuanto a vasopresores se refiere, tenemos como top 1 la Norepinefrina y en inótropos, por disponibilidad en nuestro país la Dobutamina. Aunque en estos últimos la evidencia va hacia el uso de otros inótropos como la Milrinona o Levosimendan que los veremos más adelante.
- Evidencia: SOAP II (NEJM 2010; 362: 779-89) compara Dopamina con Norepinefrina en Shock Séptico en donde se demuestra un 24% de arritmias, principalmente Fabricación auricular, vs un 12,4% en Norepinefrina y mayor mortalidad en subgrupo con Dopamina en contexto de Shock Cardiogénico. Posteriormente en Crit Care Med 2012 Vol. 40, Nº3 se confirma lo reportado anteriormente con un riesgo mayor de mortalidad con el uso de Dopamina.
- Con respecto a Adrenalina vs Norepinefrina no hay mayores diferencias estadísticas entre uno vs otro aunque se ha descrito mayor consumo de O2 miocárdico e hiperlactatemia con el uso de Adrenalina.
- Vasopresina vs Norepinefrina: El reciente estudio VANISH (JAMA 2016; 316(5): 509-18) describe algunos beneficios como menor tasa de Hemodiálisis con el uso de Vasopresina (25,4% vs 35,3% OR 0.4) aunque se desconoce el rol de otras intervenciones, por lo que no define el uso futuro de Vasopresina por sobre Norepinefrina.
- Veremos las dosis correspondientes:
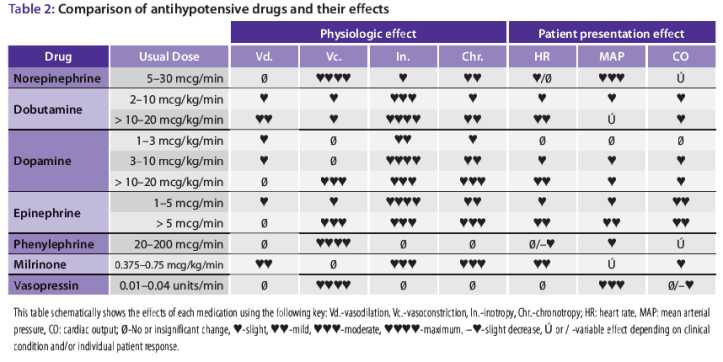
- ¿Cómo y donde funcionan los vasopresores?
- Norepinefrina: Primer vasopresor, hidroxilato derivado de la Dopamina, estimula receptores alfa y beta. En dosis terapeuticas predominan los efectos alfa. A nivel venoso, los beneficios son similares a los bolos de fluidos, es decir, pueden aumentar la precarga. Efecto inotrópico moderado por actividad beta-1.
- Comparado con Dopamina tiene un 11% absoluto de menor mortalidad, además riesgo doble de arritmias (2.34 veces).
- Uso prolongao puede ser tóxico para miocitos cardiacos –> Bradicardia refleja, arritmia cardiaca, isquemia tisular que lleva a una profunda vasoconstricción.
- Epinefrina: Agonista alfa y beta no selectivo recomendado en sepsis + hipotensión como primera alternativa o asociado a Norepinefrina. 1a linea como vasopresor en PCR, también recomendada en bradicardia.
- Dosis: 0,01 – 0,2 ug/kg/min. Dosis bajas más efectos beta, desde 0,1 ug/kg/min efectos mayores a nivel de contractilidad cardiaca y FC. Dosis elevadas efectos alfa-1 mediados –> Vasoconstricción.
- Ojo con modificaciones en pH, Lactato, glicemia!!!! (acidosis, hiperlactatemia, hiperglicemia).
- Vasopresina: Péptido hormonal endógeno que produce contracción de musculatura lisa vascular en los receptores V1, a nivel principalmente de circulación esplácnica.
- Vasopresor no adrenérgico de eventual uso como adjunto en shock séptico.
- Condiciones normales –> Responsable de homeostasis, moderada vasoconstricción a nivel de arterias pulmonares y renales.
- En muy bajas dosis vasodilatación a nivel pulmonar con liberación de óxido nítrico –> Beneficio en falla aguda de Ventriculo Derecho.
- Beneficio principal en hipotensión: Vasoconstricción y aumento de presiones sistólica y diastólica.
- Dopamina: Recomendada en shock séptico con baja sospecha de inicio de arritmias en general. No de primera linea.
- Actúa a nivel de receptores dopaminérgicos pre y post-sinápticos, localizados a nivel coronario, cerebral, renal y circulación esplácnica. Incrementa flujo plasmático a nivel renal y natriuresis.
- No diferencias en mortalidad, AKIN, TRR con «dosis renal» por lo que ya no se utiliza (Lancet 2000; 356 (9248): 2139-43, Am J Med 1999; 107 (4) 392-5).
- Dosis inicial: 2 – 10 ug/kg/min –> Predominan efectos beta-1(inotropismo, dromotropismo, cronotropismo). 10 – 20 ug/kg/min predominan efectos alfa 1 (incremento de RVP y PAM).
- Fenilefrina: Agonista alfa-1 puro. Sólo uso en circunstancias especiales que incluyen: Alto riesgo de arritmias con uso de Norepinefrina, GC alto con hipotensión persistente, hipotensión refractaria a vasopresores.
- Incrementa tono vascular venoso y arterial en dosis terapeuticas lleva a rápidos cambios en la PAM.
- Uso ideal en bolos para una respuesta rápida para corregir la hipotensión vasodilatadora (vagal por ej.).
Inótropos.
- Utilizados para aumentar el Gasto Cardiaco y la resistencia vascular sistémica baja.
- Disfunción miocárdica en sepsis es frecuente y puede explicar la baja del GC, además el flujo coronario se encuentra elevado en sepsis con mayor consumo de O2, se traduce en alteraciones del metabolismo celular y cambios en la autoregulación a nivel de microvasculatura cardiaca generan la alteración de la contractilidad en sepsis.
- Uso: Disfunción miocárdica, bajo GC, incremento de presiones de llenado, signos de hipoperfusión con adecuado volumen intravascular y PAM adecuada con fluidos y vasopresores.
- Idealmente usar inótropo que aumente contractilidad sin aumentar mucho el consumo de O2 y disminuir las presiones de llenado.
¿Cuales hay disponibles?
- Dobutamina: Derivado dehidroxilato del isoproterenol, con actividad agonista Beta-1 y en menor medida beta-2; también efecto medio alfa-1 agonista (> a 15ug/ki/min). Vida media de 2 minutos.
- Inótropo de 1a linea en SSC.
- Efectos cronotrópicos, dosis bajas pueden llevar a arritmias malignas por aumento de consumo de O2.
- Taquicardias supraventriculares y ventriculares (ojo, frecuentes).
- Milrinona: Inodilatador no adrenérgico que actúa a nivel de inhibidor de fosfodiesterasa 3 y aumento de AMPc. Vida media de 2 – 4 horas, mayor en falla renal.
- Mayor liberación de calcio a nivel de retículo sarcoplásmico –> Ca ++ en citosol –> Aumento contractilidad.
- Mayor actividad AMPc en vasculatura periférica –> Vasodilatación.
- Uso: Shock Cardiogénico con falla de VD, Milrinona disminuye resistencia vascular pulmonar,
- Uso cuidadoso en pacientes con intravascular depletado, optimizar primero!.
- Recomendado en pacientes usuarios de beta-bloqueadores.
- Levosimendan: Inodilatador sensibilizador del calcio a nivel de miofilamentos. Vasodilatador activo a nivel pulmonar, coronarias, vasculatura periferica mediado por canales de potasio en la musculatura lisa. Unión celular prolongada de calcio intracelular a troponina C cardiaca que aumenta la contracción de los miofilamentos sin incrementar la amplitud del transito de calcio.
- Ojo en sepsis: Homeostasis de calcio a nivel cardiaco se encuentra alterada por exposición a endotoxinas que alteran la relación fuerza de miofilamento – relación de calcio, daño a nivel de lipo-polisacaridos que empeoran contractilidad, ciclo rápido de calcio por mayor consumo de O2, disminución de sensibilidad de miofilamentos por el Calcio.
Conclusiones:
- ¿Cuando iniciar? Posterior a reanimación con fluidos, con intravascular adecuado evaluado mediante predictores dinámicos de respuesta a volumen y persiste PAM < 60 o < 30 mmHg de caida por debajo del basal.
- ¿Cúal? 1ª línea Norepinefrina.
- Si hay evidencia de Shock Cardiogénico de preferencia usar Norepinefrina, menor mortalidad que Dopamina en este escenario (NEJM 2010; 362: 779-89).
- Si Shock Anafiláctico: Adrenalina.
- Si Shock Séptico con bajo Gasto Cardiaco y adecuada reanimación con volumen: Evaluar uso de Dobutamina como 1a opción.
- Si Shock Obstructivo: Mejorar primero la causa, se sugieren vasopresores y evitar uso de inótropos.
- ¿Qué dosis? Norepinefrina desde 0,1 ug/kg/min, no hay una dosis tope descrita aunque se sabe que mayor a 0,3 ug/kg/min ya la mortalidad es tan alta como un 60% o más.
- Tambien recomendado las «push dose pressors»: Epinefrina 1mg/10ml SF es equivalente a 10 mcgs/ml o la mas conocida es: 1ml de Epinefrina diluido en 10cc SF, luego tomas 1ml de ellos y más 9cc de SF podemos obtener 100mcrg/ml. Dosis de 0,5 – 2 ml IV cada 2 – 5 min, duración 5 – 10 min.
- Fenilefrina: En jeringa de 3 ml, tomar 1ml de Fenilefrina, luego diluir en 100 ml SF, entonces cada ml tiene 100mcgs/ml. Dosis: 0,5 – 2ml c/ 2 – 5 min, duración 10 – 20 min. (https://emcrit.org/wp-content/uploads/push-dose-pressors.pdf).
- ¿Metas? PAM 65 – 70 hasta 75, es decir garantizar una adecuada presión de perfusión renal. En neurocríticos PAM 80 – 90. Recordar estudio SEPSISPAM 2014 (NEJM 2014; 370 (17): 1583-93) en donde se muestra mayor incidencia de arritmias con PAM 80 – 85 en Sepsis.
- ¿Complicaciones? Hipoperfusión de extremidades, mesentérica. Disrritmias. Isquemia miocárdica. Necrosis de la piel por extravasación periferica. Hiperglicemia.
- Por último se recomienda como lectura complementaria: Vasopressor and Inotrope Use in Canadian Emergency Departaments: Evidence Based Consensus Guidelines. CJEM 2015;17 (S1): 1-16.

[…] En el manejo de pacientes críticos es común la necesidad de emplear medicamentos que modifiquen el perfil hemodinámico del enfermo (vale decir, drogas vasoactivas), tanto en la Urgencia, Pabellón y UCI para asegurar una adecuada perfusión orgánica (revise nuestro artículo de uso de drogas vasoactivas aquí). […]
Me gustaMe gusta
Hola! me podrías indicar cual es la referencia del la tabla comparativa de las distintas DVA?
Muchas gracias!
Me gustaMe gusta
Por supuesto.
https://www.jems.com/2014/09/15/use-antihypotensive-medications-shock-pa/
Me gustaMe gusta
Hola me pueden enviar información y referencias sobre el manejo de push dose.
Me gustaMe gusta
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5052865/
Me gustaMe gusta