Afección a saber de gran importancia para todos los que hacemos esta maravillosa tarea que es la Medicina De Urgencia, principalmente por la gravedad del cuadro, así que, al saber reconocer oportunamente, podriamos con nuestras intervenciones, disminuir la tasa de complicaciones futuras.
Introducción.
Descrito en la literatura como un «subtipo» de ACV Hemorrágico y que corresponde a 3% de todos los ACV. La mortalidad varía desde los 22 – 50% con un 21% de riesgo de muerte a las 24 horas con un incremento hasta 37% a los 7 días y 44% a los 30 días.
Mortalidad descrita en el prehospitalario 12 – 15%.
Los factores de riesgo incluyen historia familiar de HSA (especialmente de primer grado), HTA, Tabaquismo, uso de Cocaina u otros simpaticomiméticos, Aneurisma conocido mayor de 7 mm y presencia de aneurisma en la comunicante posterior o circulación posterior.
Fisiopatología.
- Predisposición familiar.
- Enfermedades del Tejido Conectivo como: Neurofibromatosis Tipo I, Sindrome Ehlers – Danlos, Enfermedad Poliquistica Renal, Sindrome Marfan –> Se describen defectos congénitos asociados a alteraciones en la estructura de la pared arterial.
- Consecuencias de Enfermedad Aterosclerotica, dinamicas de flujo y estres de la pared muscular arterial –> Presencia de Aneurismas alrededor de puntos de alta turbulencia y/o alta oscilación de flujo.
- En suma: Las alteraciones del flujo más la debilidad de la pared arterial facilitan la formación y expansión de Aneurismas hasta el punto que exceden la fuerza de la pared del vaso, con la consecuente ruptura y hemorragia hacia el parénquima o el espacio subaracnoideo.
Etiología.
- Aneurismática.
- No Aneurismática.
- Traumática.
Aneurismática:
- Aproximadamente el 5% de todos los ACV.
- Incidencia de 10,5 personas/100.000 personas al año.
- Mujer 1,6 veces más incidencia.
- Autopsias: 1 – 5% incidencia en adultos (Aneurismas).
- Mortalidad 32 – 67%, 25% muere antes de las 24 horas y 40 – 60% fallecen antes de los 30 días.
- 10 – 20% dependencia (mRs 3 o más).
- Excluir el Aneurisma es el tratamiento más importante.
No Aneurismática (NA):
- HSA Perimesencefálica: Patrón específico de localización de sangre en el TC, Angiografía normal, hasta 2/3 pacientes con HSA NA.
-
- Sangre en cisternas perimesencefálica anterior al Tronco encefálico. Puede ser extensión de partes basales de las cisuras de Silvio pero no las laterales, cisura interhemisferica anterior o ventriculos laterales.
- Aneurisma Oculto: Descrita dentro de este grupo porque inicialmente la Angiografìa está normal (hasta 24%) y se encuentra aneurisma en la Angiografía siguiente –> Aneurismas pequeños, Vasoespasmo, Hematoma, Trombosis junto al Aneurisma.
- Malformaciones Vasculares: < 10%, pueden ser intracraneales o espinales.
-
- Intracraneal: Lesiones Congénitas, MAV, Fistula A-V dural. También Malformaciones del Seno Cavernoso, Angiomas venosos, Telangectasias capilares.
- Espinal: 10% de malformaciones espinales pueden presentar HSA. Fistula A-V dural más común.
- Disecciones Arteriales Intracraneales: 4,5% de los casos. Caracteristicamente hay hemorragia intramural que diseca entre la adventicia y la media. Formación de trombos –> ACV tromboembólico. Sangrado, habitualmente masivo, resangrado entre un 40 – 60% siempre antes de las primeras 24 horas.
-
Las describiremos con detalle en otro capítulo.
- Otras Causas:
-
- Trombosis de Seno Venoso: Rara, presentación más lenta y superficial.
- Enfermedad de Células Falciformes: Reportes de casos en niños, uno o más Aneurismas, presencia de vasos colaterales frágiles.
- Trastornos de la Coagulación o uso de TACO: HSA Perimesencefálica por lo general, puede ser mayor debido a la alteración de actividad plaquetaria.
- Apoplejia Pituitaria: Cefalea en trueno más vómitos, HSA puede ser distractora del adenoma hipofisiario. Recordar presencia de cambios de visión paresia de nervios extraoculares.
- Abuso de Cocaina: Asociado a HSA NA y Aneurismática. Sangrado relacionado por presión sanguínea y presencia de vasculopatía tóxica o hipertensiva. Siempre buscar lesión aneurismática.
- Angiopatía por Amiloidosis: Sangrado escaso generalmente, surco único.
- Tumores.
- Enfermedad de Moyamoya.
- Vasculitis, PRES, leucoencefalopatía posterior reversible.
Clínica.
- Cefalea En Trueno.
- Convulsiones (6 – 16%), compromiso de conciencia, vómitos.
- Cefalea Centinela en el 50% de los casos (Cefalea en trueno de corta duración entre 3 – 7 días previos, resolución espontánea).
- Examen Neurológico puede ser normal inicialmente.
Diagnóstico.
- Anamnesis, examen físico.
- ECG
- TC Cerebro sin contraste.
- PL.
- RNM Cerebro.
- Angiografía convencional o por Tomografía Computada.
- Doppler Transcraneal.
- Scores.
—————————————————————————————————————————————
- EGC: Recordar eje Cerebro – Corazón, cambios electrocardiográficos con buena función cardiaca, arritmias, SDST (Takotsubo).
- TC Cerebro: Imagen de entrada en este contexto con recomendaciones que se describen en 2008 American College of Emergency Physicians y se reafirman en el 2016 (Emerg Med Clin N Am (2016) http://dx.doi.org/10.1016/j.emc.2016.06.003). En sospecha HSA:
-
- A las 6 horas con una S: 92%/E: 99%
- Día 2: 85 – 95%
- Día 3: 75%
- Día 5: < 50%.
- Recordar que un 2% aproximadamente son falsos negativos.
- RNM Cerebro: Estudios limitados, sirve el FLAIR y T2 con alta sensibilidad en los pacientes con presentación subaguda (> 4 días de HSA).
- Punción Lumbar: Se recomienda realizar lo antes posible post TC, aunque debemos tener en consideración que la Xantocromía aparece entre las 6 – 12 horas y permanece hasta 2 semanas post «inicio» HSA.
-
- Debemos buscar: Inspección Visual, Presión (si no logramos medir presión no debe ser menor a 1 gota cada 2 – 3 segundos), Proteínas, Glucosa, Células, Xantocromía.
- Xantocromía aparece 6 – 12 horas posterior a inicio de cefalea puesto que es el tiempo que se demora en aparecer la degradación de la Hb (Oxihemoglobina y Bilirrubina) en LCR.
- Otras causas de Xantocromía: Elevadas concentraciones de Proteinas en LCR, Hiperbilirrubinemia ( >10 – 15 mg/dl), PL traumática con más de 100.000 cell/microL.
- Angiografía por Tomografía Computada: Se recomienda actualmente como parte del estudio inicial en los centros en los que se encuentre disponible por la posibilidad de encontrar Aneurismas en la base del craneo. De todas maneras igual se recomienda si es negativa, la Angiografía convencional. También se puede observar un «spot sign» asociada a riesgo de expansión de hemorragia o resangrado en pacientes con hemorragia intracraneana, no en HSA.
- Angiografía convencional: Incluye reconstrucción 3D, mejor caracterización de morfología, orientación, tamaño, vasos adjuntos u otro adicional al aneurisma.
- Doppler Transcraneal: Evalua la velocidad del flujo cerebral para así constatar vasoespasmo, si llegase a constatarse éste con disminución de PPC se promueve la terapia «Triple H» con eficacia muy cuestionable actualmente.
Scores.
Tratan de establecer severidad del cuadro y guiar el manejo en base a éstos, pronóstico, comparar entre grupos de similares características.
- Glasgow Coma Score: Creado en los 70’s, si bien no es una escala de HSA, se ha estandarizado en la actualidad para evaluación del estado de conciencia en casi todas las patologías neurológicas y no neurológicas que comprometen este item. Se realizó una serie prospectiva de GCS con HSA con alta correlación post cirugía (Neurosurgery 1996; 36 (1): 19), aunque la correlación mayor es entre GCS 14 – 15 no así en los otros.
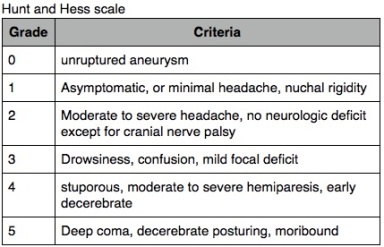
- Hunt and Hess: Propuesta en 1968, una de las más utilizadas. Intenta entregar un índice de riesgo quirúrgico, además de correlacionar la clínica inicial con la severidad de la hemorragia. Posteriormente se agrega el grado 0. Varios estudios y metaanalisis han tratado de validarlo posteriormente y se ha demostrado mejor correlación con pronóstico a los 6 meses que GCS y WFNSs aunque con bajo valor en sensibilidad/especificidad.
- World Federation of Neurological Surgeons grading score (WFNS): Propuesto en 1988, está basado en el GCS + presencia de déficit motor. Dos metaanalisis han demostrado buena correlación entre el grado WFNS y pobre pronóstico (Neurosurgery. 2004;54(3):566.), aunque hay otros que han descrito que no hay tanta correlación (Acta Neurochir (Wien). 2001;143(7):665). Está en fase de revalidación en conjunto con la Japan Neurosurgical Society.
- Escala Fisher: Descrita en 1980 como un índice de riesgo de Vasoespasmo sin resultado clínico y se describe con el patrón de hemorragia del TC inicial. Fue validado en base a un estudio pequeño prospectivo de 41 pacientes con una excelente correlación (Neurology. 1983;33(4):424).

- Escala TC Claassen: Propuesta en 2001 como índice de riesgo de isquemia cerebral secundaria a vasoespasmo post HSA, no clínica. No tiene estudio prospectivo de validación y algunos autores la describen como la Escala Fisher Modificada. Incluye presencia de HSA y hemorragia intraventricular.
-
- No HSA o HIV
- Mínima HSA sin HIV
- Mínima HSA con HIV
- HSA gruesa (llena completamente una cisura o cisterna) sin HIV
- HSA gruesa con HIV.
- «The Vasograde»: No tiene traducción pero trata de darle un color (como Triage Start) y suma las escalas de WFNS y mFs (Escala de Fisher modificada) al ingreso al SU, es bastante útil pero no está validado.
-
- Verde: WFNS 1 – 2 y mFs 1 – 2.
- Amarillo: WFNS 1 – 3 y mFs 3 – 4.
- Rojo: WFNS 4 – 5 y cualquier mFs.
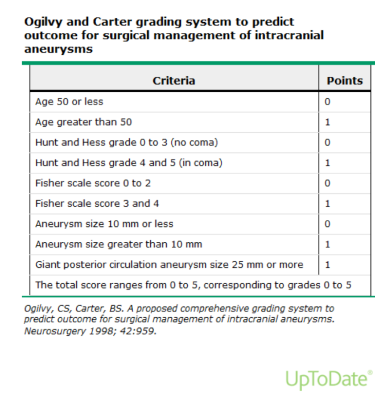
- Sistema de estradificación Ogilvy y Carter: Propuesta en 1998, estradifica pacientes en base a la edad, escala Hunt and Hess (clínica), escala Fisher (Volumen HSA y riesgo de vasoespasmo), y tamaño del Aneurisma. El rango va del 0 – 5, trata de mitigar toda la subjetividad inherentes a las escalas, validación prospectiva pequeña (Neurosurgery. 1998;42(5):959).
Manejo.
- El tratamiento más importante es EXCLUIR el Aneurisma (en el contexto de HSA Aneurismática claramente).
- Siempre ABCDE.
- Secuencia de Intubación Rápida: La indicación formal es GCS < 8, PIC elevada, pobre oxigenación, hipoventilaciñon, inestabilidad heodinámica y requerimientos de sedación/parálisis. Siempre debemos tratar de estabilizar a nuestro paciente y antes de SRI evitar a los «4 jinetes del Apocalipsis» (Hipoxemia, Acidosis, Hipotensión, Falla del VD).
- Objetivos: Evitar la inestabilidad hemodinámica y el deterioro neurológico, se describe que hasta el 35% del peor desenlace ocurre dentro de las primeras 24 horas.
- Medidas de Neuroprotección general: O2, CO2, Glicemia, cama 30º, cabeza linea media, etc.
Manejo Servicio de Urgencia.
- Control de Presión Arterial:
-
- Guias AHA 2012 –> < 160 mmHg PAS.
- Se ha descrito en Hemorragia Intracraneal (INTERAC – II, ATACH – II) presiones sistólicas hasta 129 mmHg que inclusive se han extrapolado par HSA. Sin embargo hasta ahora se mantiene el manejo de PAS en base a guías AHA.
- Para este objetivo: Betabloqueadores (Labetalol), Nicardipino, Captopril.
- Labetalol: Bolos de 10 – 25 mg en 1 – 2 minutos con repetir la dosis (si es necesario) cada 10 – 20 minutos. BIC descrita de 2mg/min (2ml/min) con dosis tope de 10 mg/min. Dosis máxima día 300 mg hasta 400 mg.
- Urapidil (disponible en algunos centros solamente): Dosis de 10 – 50 mg (dosis recomendada de 12,5 luego 25 mg) IV lento en bolo y repetir a los 5 minutos si es necesario. Se puede dejar en BIC entre 4 – 8 mg/hr (250mg/500ml SF).
- No uso de Vasodilatadores como Nitroprusiato o Nitroglicerina por incremento de volumen de sangre cerebral –> incremento de PIC.
- Ojo con bajar PAS rápido y por debajo de lo recomendado –> Riesgo de Isquemia o Resangrado.
- PAS recomendada 90 – 140 mmHg, PAD 70 – 90 mmHg.
- Mantener PPC (Presión de Perfusión Cerebral) ojalá en 70 mmHg, esto es en base a la primisa PAM – PIC.
- Control de PIC:
-
- Es muy importante ya que esto se traduce en Hidrocefalo agudo e hiperemia reactiva post hemorragia.
- Ventriculostomía –> Ventrículos aumentados de volumen o WFNS > 3. Medición de PIC y drenaje de LCR cuando es apropiado. No hay consenso si instalar en lado sano o en penumbra.
- Si no hay Ventriculostomía, manejo de Neuroprotección standard y manejo farmacológico: Solución Hipertónica, Osmoterapia. Se recomienda no hiperventilar dentro de las primeras 24 horas por el riesgo de vasoespasmo.
- Sol. Hipertónica: Descrita en pacientes con PIC elevada 2o a TEC como terapia de manejo de PIC con el objetivo de mejora PPC.
- Craniectomía descompresiva: Menos frecuente que se utilice en este escenario, ayuda al manejo de control de PIC.
- Antiepilepticos: Utilizados para prevenir convulsiones, evidencia discutida. Aunque recordar siempre: «es mejor dar anticonvulsivantes para evitar daño Neurológico por convulsiones y por disregulación cerebral». Con respecto al uso de Fenitoina, ésta puede empeorar el pronostico neurológico y cognitivo según la última evidencia, por lo que se debe reservar su uso. En ese contexto se recomienda el uso de Levetiracetam IV, dosis de 250 mg c/12 horas con dosis máxima de 1500 mg c/12 horas IV.
- Antifibrinolíticos: Investigados como prevención del resangrado post HSA Aneurismática, no tienen un rol importante, desde el 2012 se incluye dentro del manejo en las guías American Stroke Association, terapia por menos de 72 horas. Impacto en la incidencia de resangrado, a los 6 meses, sin diferencias vs placebo (J Neurosurg. 2002;97(4):771). Recordar además que se asocian con mayor riesgo de hidrocefalo agudo y de isquemia cerebral tardía.
- Suspender TACO: Si utiliza anticoagulantes, la indicación «viene de cajón». Revertir con dosis de Vitamina K IV, Plasma Fresco Congelado, Concentrado de complejo protrombínico (Complejo Factor IX).
- Corticoides: No descrito como uso de rutina en HSA.
- Terapia Triple H: Inducir Hipertensión, Hipervolemia, Hemodilusión para el tratamiento del Vasoespasmo. Actualmente es una terapia muy cuestionada y no utilizada en la actualidad, ya que se ha demostrado que no mejora el pronóstico neurológico, además parece haber otros mecanismos de daño asociado asociado.
- Otras terapias:
-
- Magnesio: Como efecto Calcio Antagonista no competitivo vía unión canales de Calcio voltaje – dependientes. En HSA se ha descrito un 50% con hipomagnesemia. Evidencia no ha mostrado beneficios vs placebo. Actualmente se recomienda uso en hipomagnesemia.
- Estatinas: Se administran en contexto pueden disminuir niveles de óxido nítrico y la disponibilidad de éste a nivel endógeno por inhibición enzimática que contribuyen al vasoespasmo. Se atribuye valor neuroprotector por disminución de la excitotoxicidad glutamato-mediada, modulando la respuesta inflamatoria. Evidencia negativa a esta teoría (STASH Trial).
- Antagonistas de receptor Endotelina (CONSCIOUS-2) negativo vs placebo.
- Tirilizad.
- Eritropoyetina.
- Gliburida. (Surgical Neurology International 2017, 8:11).
Tratamiento Aneurisma.
- Exclusión Aneurisma.
- Tasa de Resangrado 3 – 4% en las primeras 24 horas y 1 – 2% por día durante el primer mes (velocidad media > 200 cm/seg)
- Ruptura asociada 70%.
- Terapia exitosa si se realiza entre las 24 – 72 horas.
Prevención del Vasoespasmo y de Isquemia Cerebral Tardía.
- Resangrado: Hasta el 80%, 4 – 10% en las primeras 24 horas y luego cae 1,5%/día hasta el mes.
- Vasoespasmo en HSA: 20 – 30%, relacionado con sustancias espasmogénicas generadas durante la lisis de los coagulos del espacio subaracnoideo. Gerenalmente no antes de los 3 días post HSA con un pick a los 7 – 8 días.
- En cuanto a la prevención del vasoespasmo se realizan 3 intervenciones:
-
- Seguimiento con Doppler Transcranial cada 48 horas desde el 3 – 14º día.
- Euvolemia.
- Nimodipino.
- Euvolemia: NO hipovolemia por riesgo de isquemia, uso de cristaloides, BH diario.
- Nimodipino: Bloqueador de canales de calcio para prevenir el vasoespasmo. Dosis de 60 mg c/4 horas para TODOS los pacientes con HSA Aneurismatica, VO, SNE. Tratamiento por 21 días. Los efectos vasodilatadores a nivel cerebral no son del todo convincentes, sin embargo ha mostrado mejorar el pronóstico vs el manejo standard en HSA.
- HIC: Sangre intra-parenquima, incidencia del 10%.
- Hidrocefalo agudo: Obstrucción a nivel del sistema ventricular (circulación).
- Convulsiones: Incidencia del 20%.
- Hiponatremia: 30 – 50% de los casos, ocurre entre 3 – 14 días, probablemente en contexto de SIADH.

En relación al uso de Fenitoína como antiepiléptico… sólo destacar que está descrito que la fenitoína interfiere en el metabolismo hepático del Nimodipino, básicamente induce el citocromo P450 (isoenzima 3A4), por lo que altera considerablemente la concentración plasmática del fármaco y por ende de su efecto, y entendiendo que el Nimodipino, es EL fármaco importante en el manejo de la HSA aneurismática, claramente al alterar su efecto se produce deterioro del outcome final de los pacientes.
Me gustaMe gusta
Se agradece el aporte!
Me gustaMe gusta